Proses
isobarik adalah proses termodinamika dimana
tekanannya konstan: ΔP = 0. Istilah ini berasal dari kata Yunani iso-, (sama), dan baros (massa). Panas dipindahkan ke sistem yang melakukan kerja
namun juga mengubah energi dalam sistem:
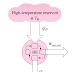
Area
kuning menggambarkan kerja yang dilakukan sistem
Menurut Hukum pertama termodinamika, dimana W adalah kerja yang dilakukan pada sistem, U adalah energi dalam dan Q adalah
panas. Kerja yang dilakukan oleh sistem tertutup didefinisikan dengan:
dengan Δ
menunjukkan adanya perubahan selama proses berlangsung, sedangkan d merupakan
lambang diferensial. Karena tekanannya konstan, maka
mengasumsikan
jumlah gas konstan (misalnya tak ada transisi fasa selamareaksi kimia), maka menurut teorema
ekuipartisi, perubahan energi dalam berhubungan dengan suhu sistem
dengan
Substitusi 2
persamaan terakhir ke persamaan pertama menghasilkan:
,
Kapasitas panas
spesifik
 merupakan indeks adiabatik atau rasio kapasitas panas. Beberapa sumber
menggunakan huruf k.
merupakan indeks adiabatik atau rasio kapasitas panas. Beberapa sumber
menggunakan huruf k.
Panas spesifik
molar isobarik:
Nilai untuk  adalah
adalah  untuk
gas diatomik seperti udara dan
untuk
gas diatomik seperti udara dan  untuk gas monoatomik seperti gas mulia. Rumus untuk
panas spesifik menjadi (untuk kasus tertentu saja):
untuk gas monoatomik seperti gas mulia. Rumus untuk
panas spesifik menjadi (untuk kasus tertentu saja):
 adalah
adalah  untuk
gas diatomik seperti udara dan
untuk
gas diatomik seperti udara dan  untuk gas monoatomik seperti gas mulia. Rumus untuk
panas spesifik menjadi (untuk kasus tertentu saja):
untuk gas monoatomik seperti gas mulia. Rumus untuk
panas spesifik menjadi (untuk kasus tertentu saja):
Proses isobarik
yang ditunjukkan pada diagram PV adalah garis lurus horizontal yang
menghubungkan keadaan awal dan akhir. Jika proses ke arah kanan, berarti ada
ekspansi, jika ke kiri, berarti terjadi kompresi.
Dalam proses
isobaric, tekanan sistem dijaga agar selalu konstan. Karena yang konstan adalah
tekanan, maka perubahan energi dalam (delta U), kalor (Q), dan kerja (W) pada
proses isobarik tidak ada yang bernilai nol. Dengan demikian persamaan hukum
pertama termodinamika tetap utuh seperti semula. Bila volume gas
bertambah, berarti gas melakukan usaha atau usaha gas positif (proses
ekspansi). Jika volume gas berkurang, berarti pada gas dilakukan usaha atau
usaha gas negatif (proses kompresi).




















0 komentar:
Posting Komentar